2020年1-4月,FDA共批准16个新药上市,其中4月份批准新药个数为5个。(此处所列新药,主要指FDA批准的新分子实体、新生物制品、细胞疗法、基因疗法,不包括疫苗)。

1.avapritinib
商品名:Ayvakit公司:Blueprint Medicines
1月9日,FDA批准Blueprint Medicines公司的Ayvakit (avapritinib)上市,用于治疗携带血小板源性生长因子受体 α(PDGFRA)基因18外显子突变的不可手术或转移性成人胃肠道间质瘤(GIST)患者,其中也包括D842V 位点突变这种最常见的18外显子跳跃突变类型。
Avapritinib是一种口服的、具有高活性高选择性的KIT及PDGFRα抑制剂。具有KIT及PDGFRα突变(包括KIT D816V、PDGFRα D842V 和KIT 外显子17突变)的多种疾病对标准疗法响应很差,缺乏有效的治疗方式,avapritinib针对以上突变在临床前均表现了很好的活性。
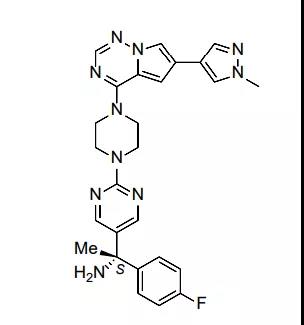
GIST是一类起源于胃肠道间叶组织的肿瘤,占消化道间叶肿瘤的大部分。GIST 可以发生于消化道的任何部位,以胃和小肠最为常见,分子机制是编码酪氨酸激酶受体蛋白基因 KIT(CD117) 或血小板源性生长因子受体 α(PDGFRα) 基因激活突变所致。大约6%的新确诊患者携带PDGFA外显子18突变。
2.teprotumumab-trbw
商品名:Tepezza公司:Horizon Therapeutics
1月21日,FDA批准Horizon Therapeutics的Tepezza(teprotumumab-trbw)上市,用于治疗甲状腺眼病。这是FDA批准的首个甲状腺眼病药物。
TED是一种常发生于甲亢患者身上的自身免疫性疾病,临床通常表现为眼球突出、复视、视力模糊和面部畸形等。该疾病主要是由于患者自身抗体激活了眼框内胰岛素样生长因子1受体(IGF-1R)所导致。
3.tazemetostat
商品名:Tazverik公司:Epizyme公司
1月24日,FDA批准Epizyme公司的Tazverik(tazemetostat)上市,用于治疗无法完全切除的转移性/局部晚期上皮样肉瘤成人患者以及16岁以上的儿科患者。
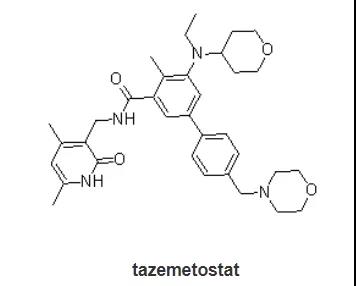
上皮样肉瘤是一种罕见的软组织肉瘤,好发于20~40岁青壮年,男性较为多见。目前,主要的治疗方案有手术切除、化疗或放疗。Tazemetostat是FDA批准的首个EZH2抑制剂,也是FDA批准的首个上皮样肉瘤治疗药物。
一项II期临床研究结果表明,接受Tazemetostat治疗的患者ORR达到15%,其中CR为1.6%,PR为13%。另外,在所有产生应答的患者中,67%的患者持续反应时间达到6个月或更长时间。
安全性方面,Tazemetostat治疗组中有37%的患者发生严重不良反应。其中≥3%的患者发生的严重不良反应主要为出血、胸腔积液、皮肤感染、呼吸困难、疼痛和呼吸窘迫。1例患者(2%)患者因情绪变化的不良反应而永久停用该药。
4.lactitol
商品名:Pizensy公司:Braintree实验室
2月12日,FDA批准Braintree实验室开发的Pizensy(lactitol)上市,用于治疗慢性特发性便秘(CIC)成人患者。
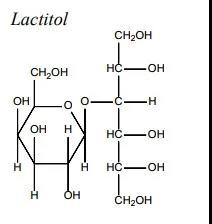
CIC是一种以排便困难、排便次数不频繁、腹痛腹胀为主要特征的疾病,在美国,大约有3500万人受到这一疾病的困扰。目前,临床上主要以包括泻药在内的药物进行治疗,这类药物虽然能一定程度缓解病人症状,但同时也带来了药物依赖。Pizensy是一种口服乳糖醇疗法,属于渗透性泻药,它能够促进水分进入肠道,进而达到通便作用。一项随机、双盲、安慰剂对照的多中心临床试验结果表明,Pizensy治疗组较安慰剂组患者在一周内达到3次完全自发排便次数(CSBMs)或者较基线比至少增加1次CSBMs的患者比例分别为25%和13%,到达主要终点。安全性方面,常见的不良反应为上呼吸道感染、腹胀、腹泻、血肌酐磷酸激酶升高、腹胀和血压升高。
5.bempedoic acid
商品名:Nexletol公司:Esperion公司
2月21日,FDA批准Esperion公司的Nexletol(bempedoic acid)片剂上市,辅助饮食和最大耐受剂量他汀用于治疗成人杂合子型家族性高胆固醇血症(HeFH)患者,或者用于需要进一步降低LDL-C的动脉粥样硬化性心血管疾病(ASCVD)患者。Nexletol是自2002年以来批准的首个每日1次口服非他汀类降LDL-C药物。
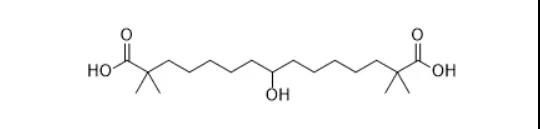
bempedoic acid是一种人工合成的二羧酸衍生物,属于first in class的ATP-柠檬酸裂解酶(ACL)抑制剂,通过抑制肝脏内胆固醇的生物合成和上调低密度脂蛋白受体(LDL-R)来降低LDL-C。
FDA批准Nexletol主要基于一系列在超过3000例患者中开展的全球关键III期项目的结果。对其中4项合计超过2600例患者的临床试验聚合分析结果显示,bempedoic acid联合中等剂量或最高耐受剂量他汀可以使安慰剂校正后的LDL-C进一步降低18%,bempedoic acid联合低剂量他汀或不使用他汀,可使安慰剂校正后的LDL-C进一步降低21%~28%。
在III期临床研究中,bempedoic acid的耐受性良好,常见不良事件的发生率与安慰剂组相似,最常见(≥2%)且高于安慰剂组的不良事件主要包括上呼吸道感染、肌肉痉挛、高尿酸血症、背痛、腹痛或轻度不适、支气管炎、贫血、肝酶升高等。不良事件严重程度方面,bempedoic acid组大多数都是轻至中度,与安慰剂组类似。
6.eptinezumab-jjmr
商品名:Vyepti公司:灵北制药
2月21日,FDA批准灵北制药的Vyepti(eptinezumab-jjmr)上市,用于成人偏头痛的预防治疗。这是FDA批准的首个预防偏头痛的静脉注射药物。Vyepti是灵北斥资19.5亿美元收购Alder公司所获得一款降钙素基因相关肽(CGRP)药物,CGRP被认为是一种与偏头痛相关的重要神经肽。Vyepti的疗效和安全性在两项随机、双盲、安慰剂对照的临床研究中得到证实。其中,PROMISE-1研究主要针对发作性偏头痛患者,PROMISE-2研究主要针对慢性偏头痛患者。结果表明,Vyepti在这两项研究中均到达了降低患者1-3个月内平均每月偏头痛天数(MMD)的主要终点。另外在一项涉及2076例患者的安全性研究表明,Vyepti最常见的不良反应为鼻咽炎和超敏反应。
7.amisulpride
商品名:Barhemsys公司:Acacia Pharma
2月27日,FDA批准Acacia Pharma公司的Barhemsys(amisulpride)上市,作为单药或联合其它疗法,治疗和预防患者术后恶心和呕吐症状(PONV)。这是首个获批的对于先前预防失败患者的术后恶心呕吐补救疗法。
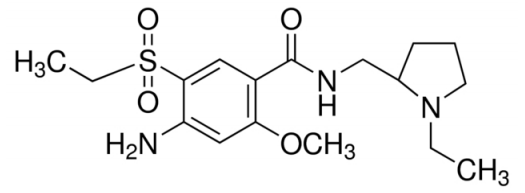
PONV是外科手术的常见并发症,大约30%的手术患者和80%的高危患者都会发生这一症状。PONV与麻醉气体或镇痛药物的使用有关,在妇科、腹部、乳房、眼睛和耳朵的手术后,尤其在持续一个小时及以上时间的手术后,更为常见。部分患者调查显示,PONV被列为手术并发症中最严重的症状之一,甚至超过疼痛。Barhemsys是一种选择性多巴胺D2和D3受体拮抗剂。Barhemsys的疗效和安全性在4项III期临床研究中得到证实。其中,一项涉及标准止吐疗法预防失败患者的的临床研究结果表明,Barhemsys治疗组治疗效果显著优于安慰剂组(42% vs 29%)。另一项涉及PONV高风险患者的临床研究结果表明,Barhemsys联合另一项止吐药的治疗效果显著由于安慰剂联合该止吐药的效果(58%vs 47%)。
8.rimegepant
商品名:Nurtec ODT公司:Biohaven公司
2月27日,FDA批准Biohaven公司的Nurtec(rimegepant)口腔崩解片上市,用于成人急性偏头痛的治疗。
Rimegepant是一种口腔崩解片(ODT),可在无水(或仅有少量水存在)的条件下于口腔中快速崩解,随吞咽动作进入消化道,在口腔内无粘膜吸收。与普通制剂相比,ODT有服用方便、吸收快、生物利用度高、对消化道黏膜刺激性小等优点,受到广泛关注。
FDA对rimegepant的批准基于一项关键的III期临床试验(Study 303)和一项长期开放标签安全性研究(Study 201)的结果。
在Study 303研究中,与安慰剂相比,在服用rimegepant后2小时,达到无疼痛和大多数烦人症状(MBS)的共同主要终点方面具有一致的统计学显著差异,rimegepant在缓解疼痛(将中度或重度疼痛减轻为无痛或轻度疼痛)和在1小时内恢复正常功能方面也显示出统计上的优势。对于大多数患者而言,疼痛自由、疼痛缓解、恢复正常功能以及摆脱MBS的益处持续了48小时。重要的是,只需1剂rimegepant就可以看到这些获益。服用rimegepant的患者中有86%在给药后24小时内不需要急救药物(例如NSAIDS,对乙酰氨基酚)。Study 201研究评估了长期多次服用rimegepant的安全性和耐受性。该研究评估了1798例偏头痛发作的患者,这些患者根据需要服用75mg的rimegepant,每天最多服用1剂。该研究包括1131例暴露于rimegepant至少6个月和863例暴露于至少1年的患者,所有这些患者平均每月至少发生2次偏头痛发作,但该研究尚未确定rimegepant在30天内出现15次偏头痛发作患者身上的安全性。在临床研究中,少于1%的受试者发生呼吸困难和严重皮疹的超敏反应,包括给药后延迟的严重超敏反应。
9.isatuximab商品名:Sarclisa公司:赛诺菲
3月2日,FDA批准赛诺菲的CD38单抗药物Sarclisa (isatuximab-irfc)上市,用于联合泊马度胺和地塞米松治疗既往至少接受过2线以上疗法(包括来那度胺和一种蛋白酶体抑制剂)的复发性难治性多发性骨髓瘤(MM)成人患者。isatuximab通过靶向多发性骨髓瘤细胞上CD38受体的特定表位促进肿瘤细胞程序性死亡,是继强生Darzalex(达雷妥尤单抗)之后全球第2款获FDA批准的CD38抗体药物。2019年,Darzalex销售额达到29.98亿美元。
此次批准是基于ICARIA-MM临床试验,结果显示,Sarclisa联合泊马度胺+地塞米松治疗组较泊马度胺+地塞米松治疗组患者的疾病进展和死亡风险降低了40%(HR 0.596),二者的中位无进展生存期(PFS)分别为11.53 和 6.47个月;同时,Sarclisa联合泊马度胺+地塞米松治疗组较泊马度胺+地塞米松治疗组患者的总体缓解率显著提高(60.4%vs. 35.3%)。安全性方面,Sarclisa联合治疗组最常见的不良反应为中性粒细胞减少症(96%)、输液相关反应(39%)、肺炎(31%)、上呼吸道感染(57%)和腹泻(26%);超过5%的患者发生严重不良反应,包括肺炎(25.3%)和发热性中性粒细胞减少(12.3%);7%的患者因不良反应(3-4级)而停用Sarclisa联合治疗,3%的患者因输液相关反应而停止治疗。
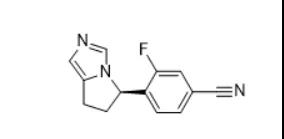
10.osilodrostat商品名:Isturisa公司:诺华
3月7日,FDA批准诺华的Isturisa(osilodrostat)上市,用于治疗库欣综合征。这是FDA批准的首个口服11‐β‐羟化酶抑制剂。
库欣综合征,又称皮质醇增多症,是一种由于多种原因引起的肾上腺皮质长期分泌过多糖皮质激素所产生的临床症候群。库欣综合征是一种罕见疾病(发病率为1~2/100万),患者通常表现为满月脸、多血质外貌、向心性肥胖、痤疮、紫纹、高血压、继发性糖尿病和骨质疏松等。
该类疾病高发年龄为20~50岁,女性发病率为男性的3倍。Isturisa是一种皮质醇合成抑制剂,可抑制11-β羟化酶的产生而起到治疗作用,11-β羟化酶是负责肾上腺皮质醇合成最终步骤的酶。研究结果表明,Isturisa可使库欣综合征患者皮质水平正常化,并改善其他临床特征。在III期LINC‐3研究中,接受Isturisa治疗的患者在停药8周后保持正常平均尿游离皮质醇的比例显著高于安慰剂(86% vs 29%)。安全性方面,常见的不良反应为肾上腺功能不全、疲劳、恶心、头痛和水肿。
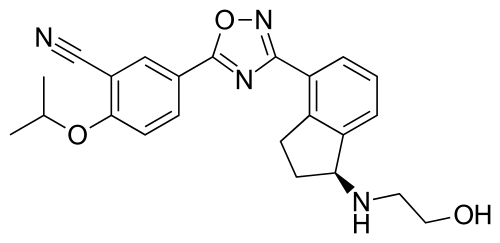
11.ozanimod商品名:Zeposia公司:BMS
3月26日,FDA批准BMS的Zeposia (ozanimod)上市,用于治疗成人复发型多发性硬化症(RMS),包括临床孤立综合征、复发缓解型多发性硬化症(RRMS)、以及活动性继发进展型多发性硬化症(SPMS)。
MS是一种人体免疫系统异常攻击大脑、脊髓、视神经的神经细胞髓鞘而引起的慢性疾病,表现为肌肉虚弱、疲劳、视物困难,最终导致残疾。全球大约有230万例MS患者,其中85%在初次确诊时属于复发缓解型MS(RRMS),15%属于原发进展型MS(PPMS)。RRMS患者表现为周期性的疾病复发与缓解,随着疾病的进展,最终会恶化成继发性进展型多发性硬化症(SPMS)。PPMS患者则表现为症状持续恶化,没有明显的缓解期。MS目前尚无法完全治愈。
Ozanimod是鞘氨醇1-磷酸受体(S1PR)调节剂,对淋巴细胞表面的S1PR1和S1PR5均有较高的亲和力。当Ozanimod与受体的结合发生后,可以阻止淋巴细胞离开淋巴结进入中枢神经系统,起到抗炎作用。此外,siponimod也能进入中枢神经系统,直接与少突胶质细胞和星形胶质细胞上的S1PR结合,促进髓鞘再生和防止炎症。
12.selumetinib商品名:Koselugo公司:阿斯利康/默沙东
神经纤维瘤病(NF)是一种良性的周围及中枢神经系统疾病,属于常染色体显性遗传病。根据其临床表现和基因定位位点不同,主要分为神经纤维瘤病1型( NF1)和神经纤维瘤病2型(NF2)。
据估计,NF1发病率大约为1/3000~4000个新生儿。大约20~50%的NF1患者可能为丛状神经纤维瘤,这种肿瘤往往不能完全手术切除,复发风险高。NF1患者可能会伴有许多并发症,如学习困难、视力障碍、脊椎扭曲和弯曲、高血压和癫痫。NF1还会增加一个人患其他癌症的风险,包括恶性脑瘤和白血病等。
Selumetinib是一款MEK 1/2抑制剂,MEK是RAS/MAPK信号通路中的关键蛋白激酶,而NF1的发病正是由于NF1基因突变扰乱了RAS/MAPK信号通路所导致的肿瘤生长。该药曾获得FDA授予的孤儿药资格和突破性治疗法称号。目前,这款药物已经在中国获批临床。
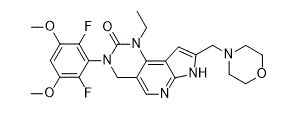
13.pemigatinib
商品名:Pemazyre公司:Incyte公司
4月17日,FDA加速批准Incyte公司Pemazyre(pemigatinib),用于治疗既往接受过治疗的携带FGFR2融合或重排的局部晚期或转移性胆管癌患者,批准时间比预定的5月30日审批日期提前了一个半月,这也是FDA批准的首个胆管癌靶向疗法。
pemigatinib结构式
pemigatinib是一种选择性的成纤维细胞生长因子受体(FGFR)抑制剂,对FGFR1、FGFR2、FGFR3均有抑制作用。FGFRs在肿瘤细胞增殖、生存、迁移、新生血管形成中发挥着重要作用。FGFRs基因的融合、重排、易位和扩增与多种癌症的发生和进展密切相关。FDA曾授予pemigatinib用于接受过治疗的携带FGFR2基因易位的晚期/转移性或不可手术切除的胆管癌患者突破性疗法资格,以及治疗胆管癌的孤儿药资格。
14.tucatinib
商品名:Tukysa公司:Seattle Genetics公司
4月17日,FDA批准Seattle Genetics公司Tukysa(tucatinib)上市,联合化疗(曲妥珠单抗和卡培他滨)用于治疗无法通过手术切除并且之前已经接受过一种以上疗法的HER2阳性晚期乳腺癌患者。这是FDA在“ORBIS计划”下批准的首个新分子实体药物,比预定审批期限提前了4个月。
FDA此次批准Tukysa主要基于一项入组612例HER2突变阳性的晚期不可手术切除或转移性乳腺癌患者的临床试研究结果,这些患者既往接受过曲妥珠单抗、帕妥珠单抗和T-DM1治疗,其中48%在入组时已经发生脑转移。研究的主要终点是无进展生存期(PFS),次要终点是脑转移患者的OS和PFS。
结果显示,与安慰剂组+曲妥珠单抗+卡培他滨治疗组相比,Tukysa+曲妥珠单抗+卡培他滨治疗组患者的中位PFS显著提高(7.8 vs 5.6个月),OS显著提高(21.9 vs 17.4个月),脑转移患者的PFS也显著提高(7.6 vs 5.4个月)。
Tukysa治疗组患者最常见的不良反应包括腹泻,手脚灼热或刺痛,恶心,疲劳,肝损伤,呕吐,口腔炎,食欲下降 ,腹痛,头痛,贫血和皮疹等。
15.sacituzumab govitecan-hziy
商品名:Trodelvy公司:Immunomedics公司
4月22日,FDA加速批准Immunomedics公司的抗体偶联药物Trodelvy(sacituzumab govitecan-hziy)上市,用于治疗既往接受过至少2种疗法的转移性三阴乳腺癌成人患者。Trodelvy是FDA批准的首个治疗三阴乳腺癌的抗体偶联药物,也是首个获批的靶向人滋养层细胞表面抗原2(Trop-2)的抗体偶联药物。
FDA此次批准是基于一项多中心、单臂、II期临床试验中的客观应答率(ORR)和应答持续时间(DoR)数据。108例既往接受过3线(中位数,范围:2~10)治疗的三阴乳腺癌患者的ORR为33.3%(95% CI:24.6%~43.1%),中位DoR为7.7个月(95% CI:4.9~10.8个月)。
Trodelvy的药品标签中带有黑框警告,提示其有严重中性粒细胞减少和腹泻的风险。II期试验中Trodelvy治疗最常见(≥25%)的不良反应包括恶心、中心粒细胞减少、腹泻、疲劳、贫血、呕吐、脱发、便秘、食欲减退、红疹、腹痛。发生率≥5%的3/4级严重不良反应包括中性粒细胞减少、白细胞计数减少、贫血、低磷血症、腹泻、疲劳、恶心、呕吐。2%的患者因为不良事件终止了治疗,未见治疗相关的死亡病例,未见严重中性粒细胞减少或间质性肺病的病例。
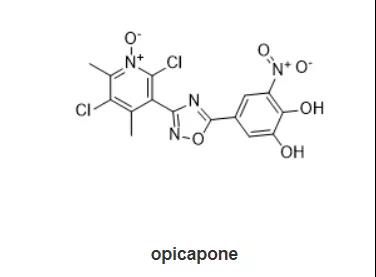
16.opicapone商品名:Ongentys公司:Neurocrine Biosciences
4月24日,FDA批准Neurocrine Biosciences公司的Ongentys(opicapone)上市,作为左旋多巴/卡比多巴的辅助疗法,用于治疗处于关闭期的帕金森患者。
帕金森是仅次于阿尔茨海默氏病的美国第二大最常见的神经退行性疾病。据估计,美国帕金森患者大约有100万例,每年新增确诊患者大约为5万例。
opicapone是一种口服选择性COMT抑制剂,能通过抑制分解左旋多巴的COMT酶,进而减少其在血液中的分解,使得更多药物到达患者大脑,最终起到延长疗效和实现患者运动功能的作用。
文章来源:白话文医药魔方Info( 医药魔方Info)
医药魔方Info)

