文章来源:药渡
激酶抑制剂分类
激酶(kinase)是一类重要的信号传递者,参与多种细胞活动,包括细胞增殖、存活、凋亡、代谢、转录、分化等。对磷酸化酶激酶特性的开创性研究始于1950年,迄今为止,在人体中已确认了518种激酶和900多个编码具有激酶活性的蛋白质的基因。激酶药理和病理学证据表明,激酶是治疗多种疾病的理想药物靶点,多年来,选择性小分子激酶抑制剂作为一种重要的抗癌药,在临床用于治疗常见的恶性肿瘤,如乳腺癌、肺癌等,取得了较好的疗效。
根据结合模式的不同,激酶抑制剂可分为不可逆及可逆两大类。前者指化合物通过与Cys反应形成共价键结合在ATP结合位点上,从而阻断ATP位点,该过程具有不可逆转性。后者根据结合口袋区域及DFG基序构象的不同,可分为四种主要的不同亚型
图1. 激酶小分子结构和分类
2017—2019迎来爆发式发展
从2001年至2019年,美国食品药品监督管理局(FDA)批准了62款抗肿瘤小分子激酶抑制剂。
近19年内,抗癌激酶抑制剂取得了长足的发展。2001年,该领域迎来第一款药物—诺华的Imatinib获得FDA批准,用于治疗胃肠道间质瘤等疾病,拉开了抗癌激酶小分子的序幕。2001至2005年,该类药物平均每年获批1款,稳步发展。2007至2011年期间共批准9款,平均每年2款,速度有所增长。2012年该类药物批准数量达到一个小高峰,而后逐渐下降至2014年的3款。2015年批准7款。2017至2019年,该类药物迎来爆发式发展,共有25种新药获得审批。
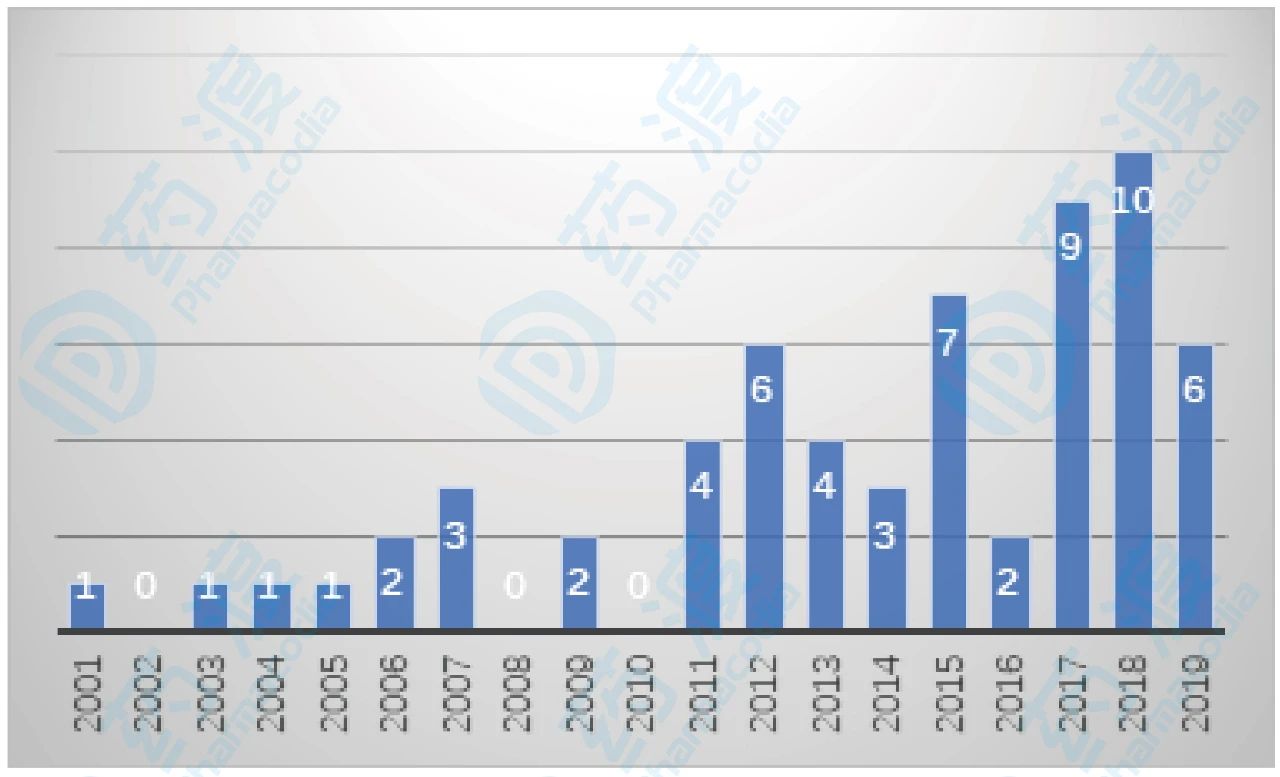
图2. 2001—2019年FDA批准的抗癌激酶小分子数量分布
分子量大多集中在400至600之间

图3. 2001—2019年FDA批准的抗癌激酶小分子分子量分布
适应症分布:白血病批准药物最多
白血病激酶小分子批准数量最多,18款
肺癌作为最常见的癌症之一,是癌症相关死亡的主要原因。近20年FDA批准的治疗肺癌的激酶小分子有14款,均是非小细胞肺癌,非小细胞肺癌(NSCLC)约占所有肺癌的 85%—90%。第一款药物是阿斯利康的吉非替尼,于2003年在美国上市,2005年,吉非替尼进入中国市场,开启了中国非小细胞肺癌靶向药物治疗的时代。
乳腺癌是全球女性最常见的恶性肿瘤之一,占女性新发癌症总数的1/4。2016年全球乳腺癌药品市场规模约达119.7亿美元,2013年中国乳腺癌市场规模约为113亿元,2017年中国乳腺癌市场约达182亿元。
2001至2019年间FDA批准的乳腺癌激酶小分子有9款,第一款是诺华的拉帕替尼,于2007年在美国上市。赫赛汀和拉帕替尼都是分子靶向药,赫赛汀仅针对HER2,拉帕替尼针对HER2和HER1,是一个多靶点的药物,且拉帕替尼是口服小分子,可能更容易通过血脑的屏障,所以治疗领域今后可能会更广。
乳腺癌领域涉及的靶点有CDK4/6等,唯一靶向mTOR的乳腺癌激酶小分子是诺华生产的Everolimus(依维莫司),于2009年在美国上市。Alpelisib是第一款PI3K抑制剂,诺华开启了乳腺癌新分子分型时代。
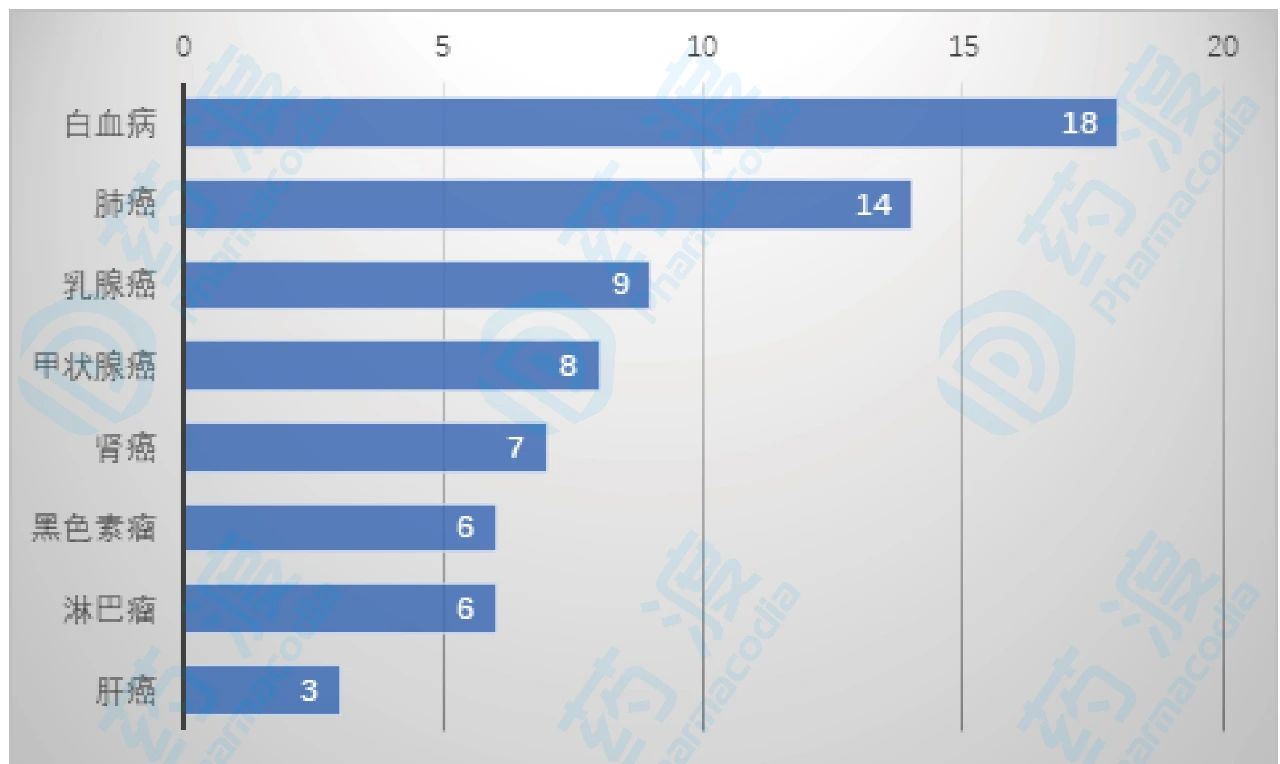
图4.适应症对应的激酶小分子数量
企业分布:诺华占据榜首,其次辉瑞
诺华获得批准的药物数量最多,为12款,占所有药物的19%。第一款抗癌激酶抑制剂伊马替尼就是由诺华生产,上市时间是2001年;2007年诺华有两款药物上市,分别是治疗乳腺癌的拉帕替尼和治疗慢性髓细胞性白血病的尼洛替尼;2017年诺华收获3款抗癌激酶小分子,分别是尼拉帕利、Midostaurin和瑞博西尼。
辉瑞位居其次,有10款获批药物。其第一款激酶小分子是2006年批准的Sunitinib (舒尼替尼),用于治疗胃肠道间质瘤等癌症;2007年批准的Temsirolimus(替西罗莫司)用于治疗肾细胞癌;2018年,辉瑞拿下3款激酶小分子的战绩,分别是Glasdegib(急性髓细胞性白血病)、Talazoparib(乳腺癌)和Lorlatinib(非小细胞肺癌)。
阿斯利康有5款激酶小分子批准,最早是2003年批准的Gefitinib(吉非替尼),用于治疗非小细胞肺癌;而后2011年阿斯利康的第二款激酶小分子获批,Vandetanib(凡德他尼) 用于治疗甲状腺髓样癌;2015年批准两款,分别是Olaparib(奥拉帕利)和Osimertinib(奥希替尼)。2017年批准的是Acalabrutinib,用于治疗套细胞淋巴瘤,慢性淋巴细胞性白血病。
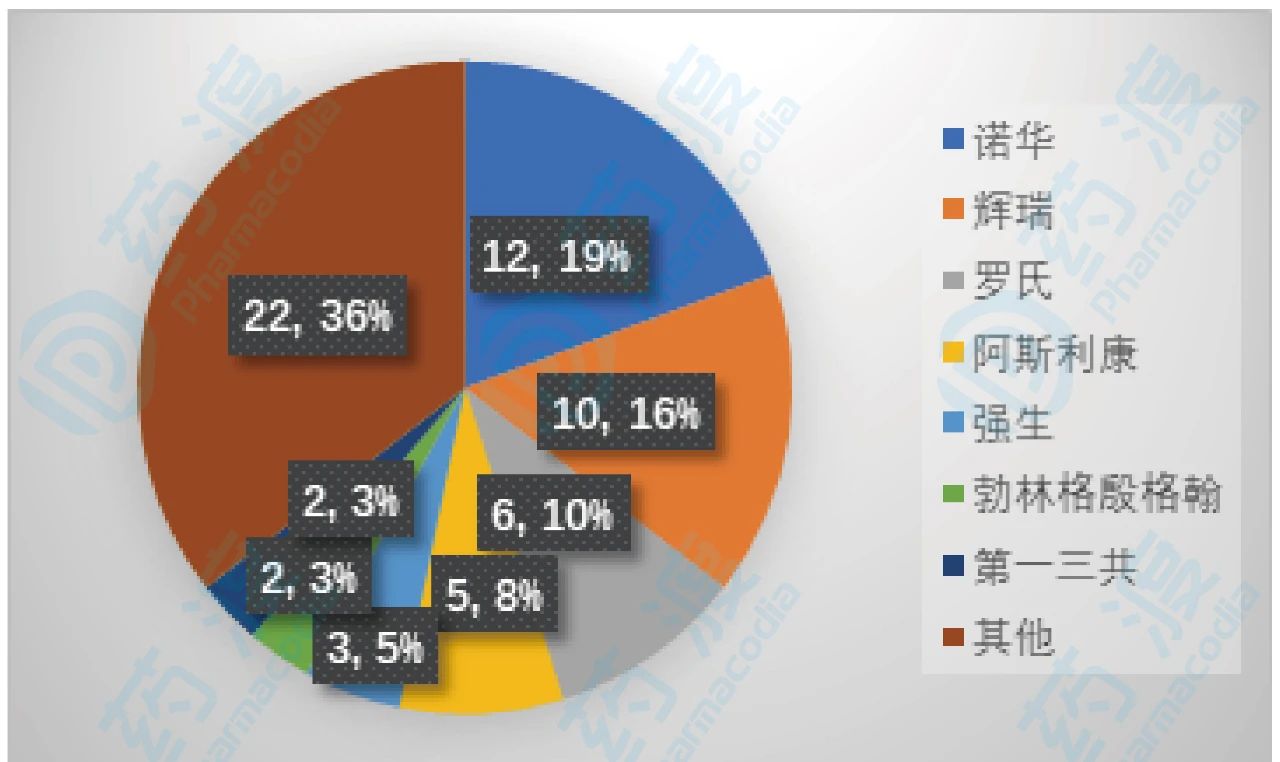
图5.部分制药企业拥有的激酶小分子数量
靶点分布

图6. 激酶小分子靶点,来自参考资料2
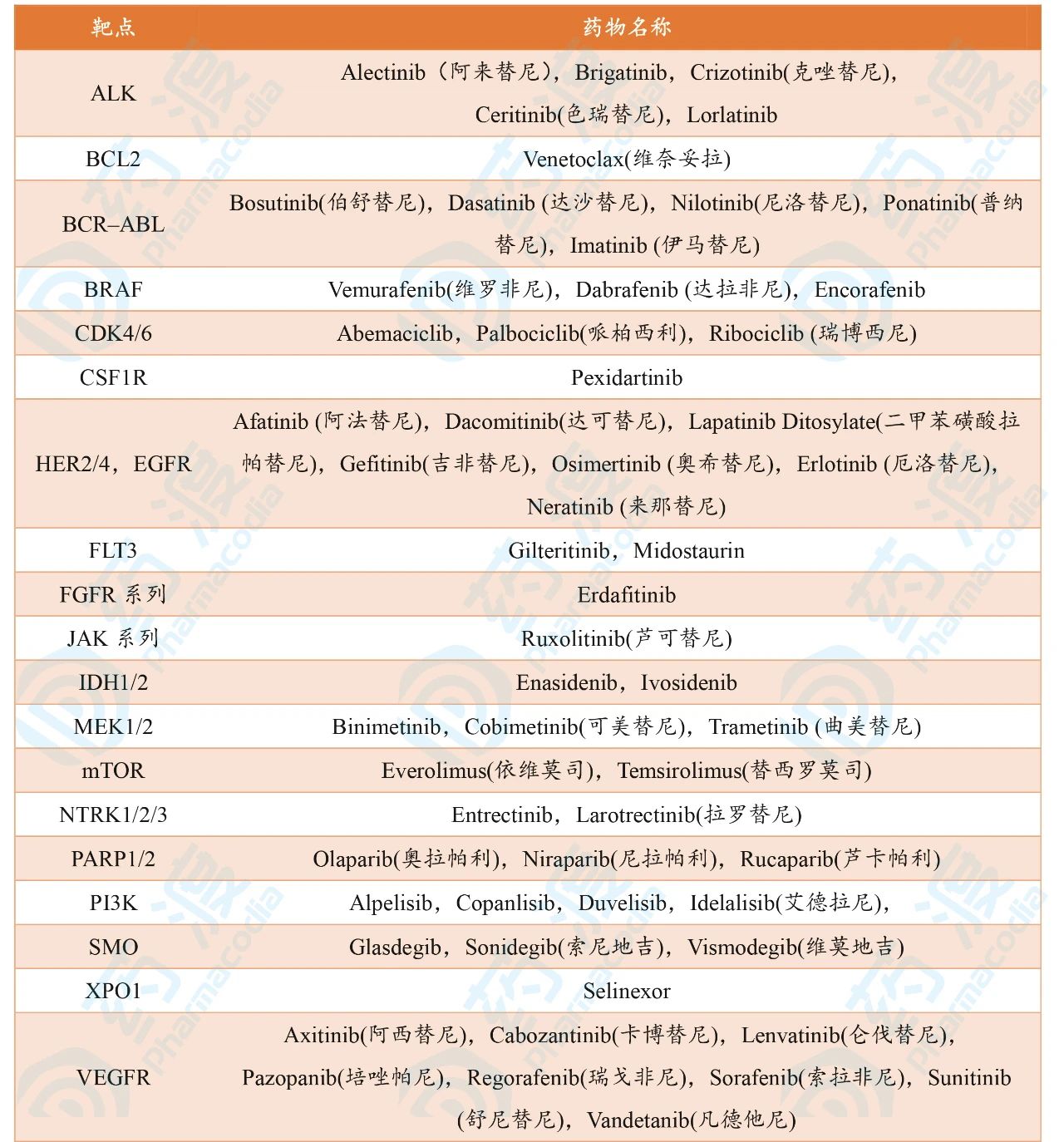
表1激酶小分子靶点及对应药物
2001—2010:11款获批
这十年内FDA共批准11款抗癌激酶小分子,具体信息见表2。
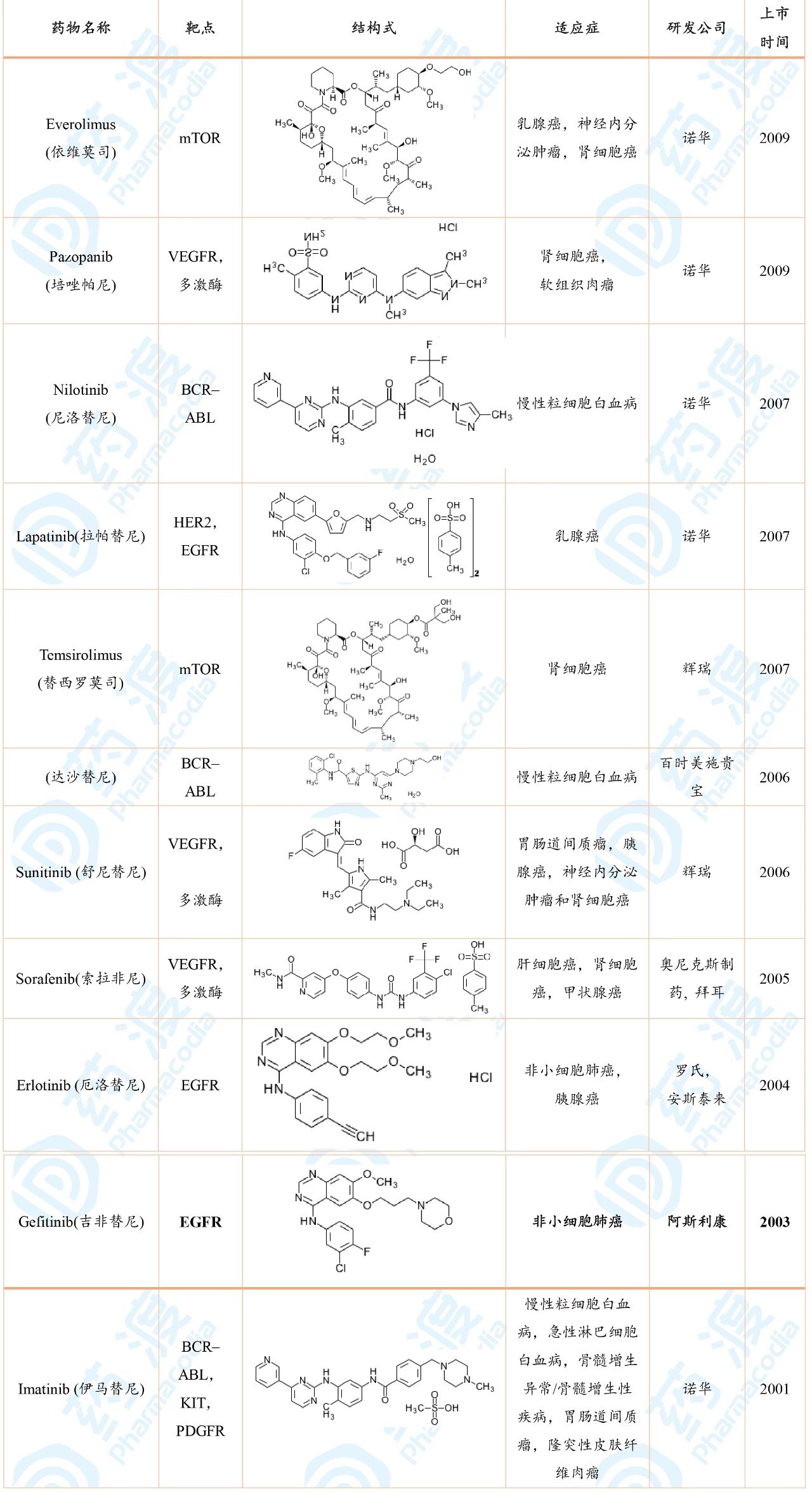
表2 2001—2010年间FDA批准的抗癌激酶小分子
2011—2015:24款获批
这五年之内,FDA批准了24款抗癌激酶小分子抑制剂,其中非小细胞肺癌治疗药物有8款
肺癌是世界上导致患者死亡数目最高的癌症类型之一,而非小细胞肺癌(NSCLC)患者占肺癌患者总数的85%,因此,针对NSCLC的疗法开发一直是癌症疗法开发的热点。
表3 2011—2015年间FDA批准的抗癌激酶小分子
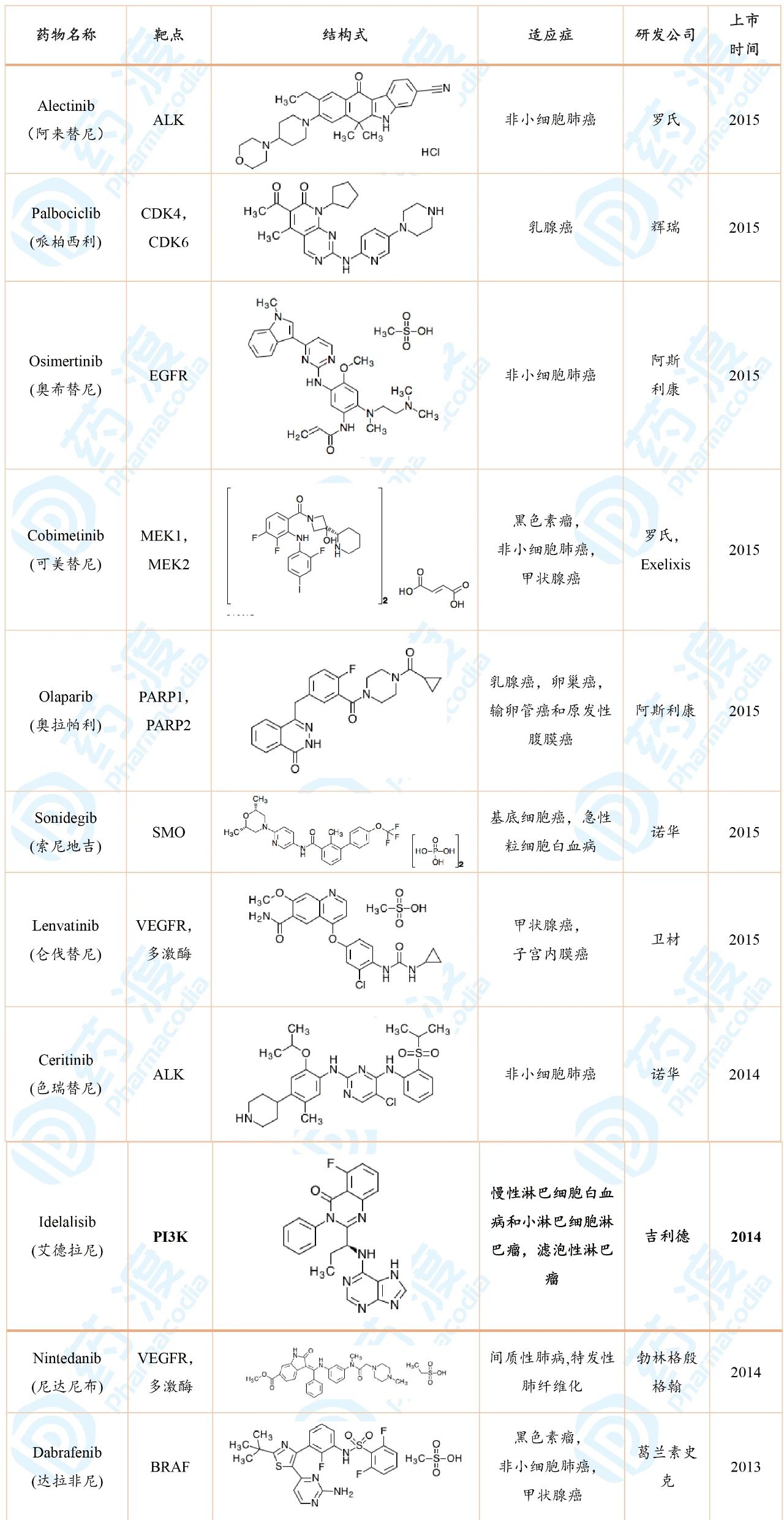
2016—2017:11款获批
此阶段批准药物的适应症最多的是白血病,其次是乳腺癌。
用于治疗白血病的药物有4款,分别是Enasidenib、Midostaurin、Acalabrutinib和Venetoclax(维奈妥拉)。
Venetoclax:全球第一个特异性靶向B细胞淋巴瘤-2蛋白(BCL2)的新型口服靶向药,于2016年经FDA批准用于治疗慢性淋巴细胞白血病(CLL)和某些类型的小淋巴细胞淋巴瘤。该品种2019年全球销售额接近8亿美元。
用于治疗乳腺癌的药物有3款,分别是Neratinib (来那替尼)、Ribociclib (瑞博西尼)和Abemaciclib。
Neratinib:FDA批准的首个HER2阴性乳腺癌泛HER抑制剂。Neratinib是一种不可逆酪氨酸激酶抑制剂,可通过阻断泛HER家族(HER1,HER2和HER4)和下游信号转导来抑制肿瘤的生长和转移。该品种于2020年5月7日在中国上市,由北海康成负责该品种大中华区的开发和商业化独占许可协议。
表4 2016—2017年间FDA批准的抗癌激酶小分子
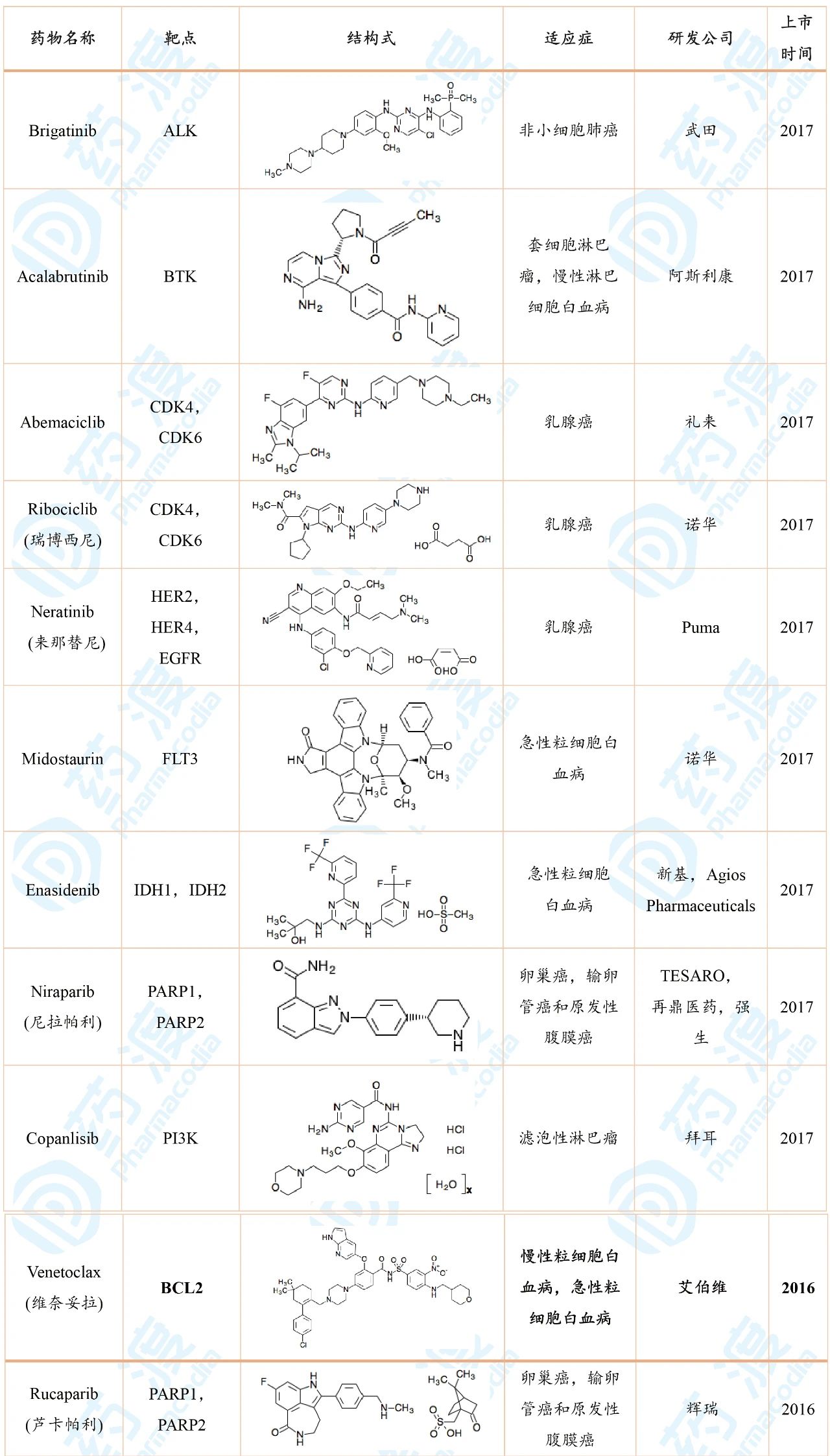
2018—2019:16款获批
这两年内批准了16款抗癌激酶小分子,具体信息见表5。
表5 2018—2019年间FDA批准的抗癌激酶小分子
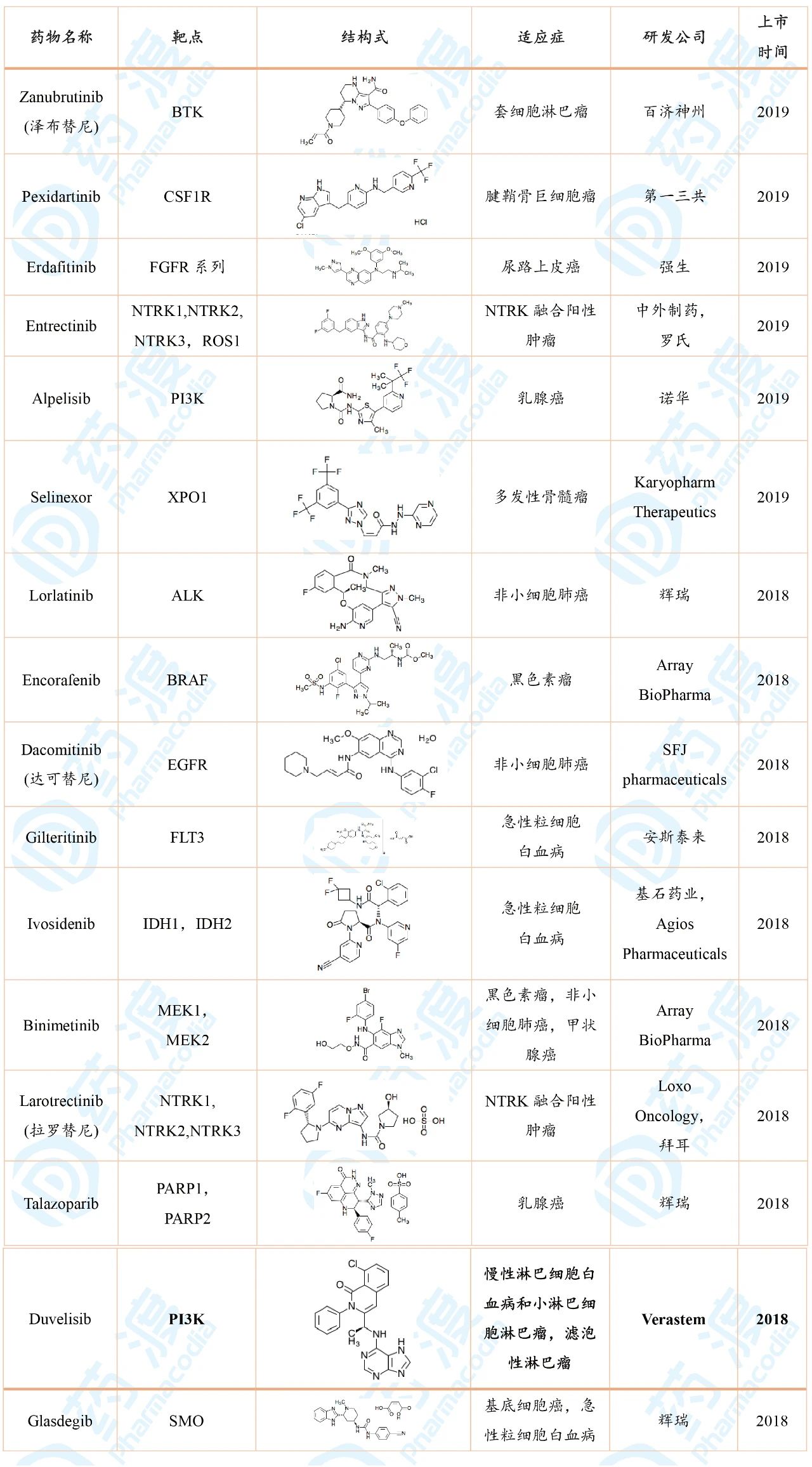
小结
激酶信号调控人体的许多的生理过程,如炎症反应、中枢神经系统异常、心血管疾病、糖尿病及癌症等,已获批药物超过90%以上集中在癌症治疗领域。针对激酶的小分子抑制剂类药物应用领域亟待拓展。
绝大多数抑制剂为可逆性抑制剂,也就是说绝大多数小分子抑制剂的作用靶点分子不止一个,这就导致药物脱靶现象以及副作用的产生。与之相随,具有绝对选择性的抑制剂分子极为稀少。具有新的作用机制及特异性的激酶抑制剂类药物有待开发。
在接下来的十年中,小分子抑制剂无疑将继续在肿瘤学中继续发挥重要作用。随着分子生物学、药物学和计算化学的进步,难成药靶点小分子新药研发已经取得了进展。小分子免疫肿瘤抑制剂,例如HPK1拮抗剂、腺苷受体、toll样受体和趋化因子受体,成为新药研发热点。
参考资料
Small Molecule Kinase Inhibitors as Anti-Cancer Therapeutics. Mini-Reviews in Medicinal Chemistry, 2012, 12, 399-411
Small molecules, big impact: 20 years of targeted therapy in oncology. Lancet 2020; 395: 1078–88
Kinase inhibitors and monoclonal antibodies in oncology: clinical implications. Nature Reviews Clinical Oncology, 2016,13,209–227

