在制药和医疗设备等行业,我们经常会被问到一个问题“Minitab 21获得FDA验证了吗?”
软件如何获得验证
这是一个很好的问题。为了满足美国食品和药物管理局(FDA)的监管要求,许多公司(包括制药和医疗设备行业的公司)必须验证其数据分析软件。这可能是一个很大的麻烦,所以为了使这个过程更容易,Minitab提供了一个验证工具包。
我们对Minitab统计软件进行了非常严格和广泛的内部测试,以确保所有统计输出的数字准确性和可靠性。有关我们的软件测试程序的详细信息,请参阅验证套件。该套件还包含一个自动化宏脚本,可在您的机器上生成各种统计和图形分析。然后,您可以将您的结果与我们在内部验证过的提供的输出文件进行比较,以确保您机器上的结果与验证结果相匹配。
预期用途
FDA法规规定,购买者必须对生产中使用的软件进行验证,或将其作为“预期使用”软件的质量系统的一部分。FDA的联邦法规21CFR820规定:“当计算机或自动数据处理系统用作生产或质量系统的一部分时,制造商应根据既定协议对计算机软件的预期用途进行验证。”
FDA在“软件验证原则”的“自动化过程设备和质量系统软件的验证”第6.3节中为医疗设备制造商提供了额外的指导。
“设备制造商有责任确保现成(OTS)软件开发人员使用的产品开发方法对于设备制造商预期使用该OTS软件来说是适当和充分的。对于OTS软件和设备,设备制造商可能或不可能访问供应商的软件验证文档。如果供应商可以提供有关其系统要求,软件要求,验证过程以及验证结果的信息,那么医疗设备制造商可以使用该信息作为他们所需验证文档的起点。“
预期用途的验证包括将软件需求映射到测试用例,其中每个需求都跟踪到测试用例。测试用例可以包含:
测试用例描述。例如,验证正态数据的能力分析。
执行步骤。例如,转到统计>质量工具>能力分析>非正常,然后输入要评估的列并选择适当的分布。
测试结果(带屏幕截图)。
测试通过/失败确定。
测试人员签名和日期。
例子说明
验证时,“预期用途”指南有充分的理由。这里是一个例子:
XYZ公司正在使用Minitab来估算制造过程中有缺陷部件的可能性。如果X部分的尺寸超过10,则认为产品有缺陷。他们使用Minitab执行功能分析,方法是选择统计>质量工具>能力分析>正态
在下图中,Ppk(1.32)和PPM(每百万37个缺陷)令人满意。
然而,这些好数字会误导制造商认为这是一个好的过程。Minitab的计算是正确的,但这个数据是非正态的,所以正态的能力分析是错误的使用过程。
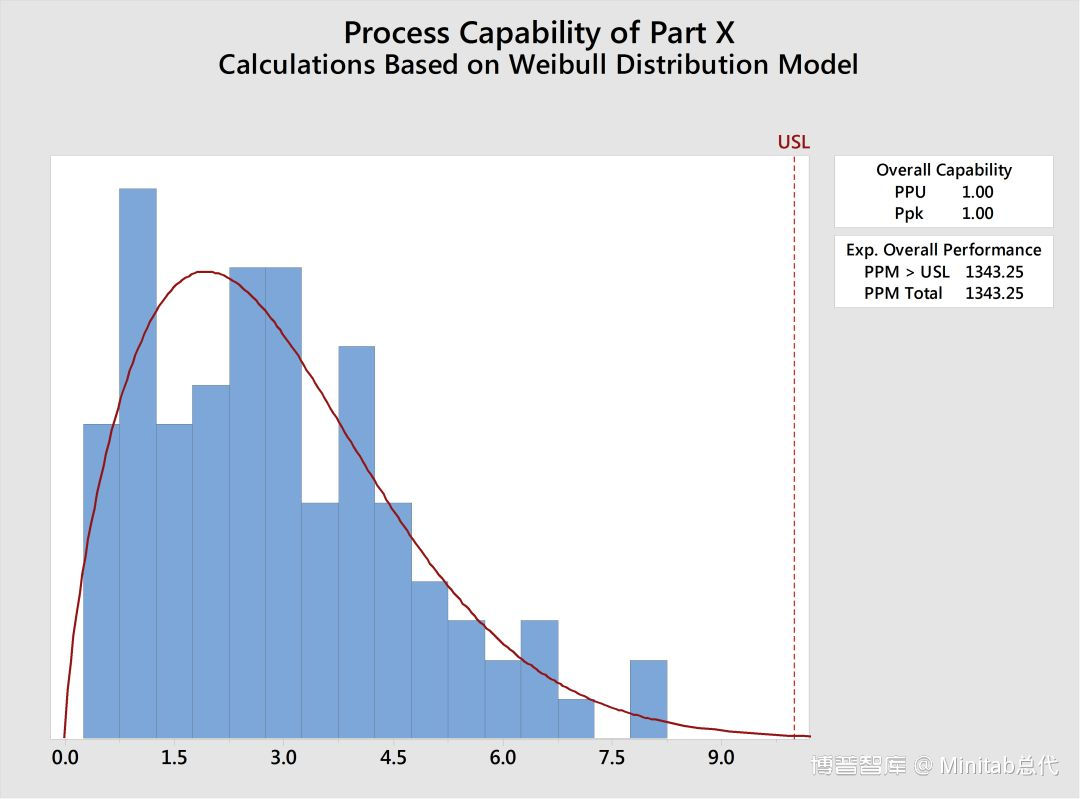
幸运的是,Minitab提供了非正态能力分析。如下图所示,如果我们选择统计>质量工具>能力分析>非正态

彻底识别,记录和验证软件的所有预期用途有助于保护制造FDA监管产品的企业和最终使用它们的人员。
Minitab提供的软件验证资源
要下载Minitab的软件验证套件,请访问http://www.minitab.com/support/software-validation/( http://www.minitab.com/support/software-validation/)
http://www.minitab.com/support/software-validation/)
除了关于我们的测试程序和用于将您的结果与我们验证的结果进行比较的宏脚本的详细信息之外,该套件还包含软件生命周期信息。
有关验证Minitab相对于FDA指南CFR标题21第11部分的更多信息,请访问此链接http://it.minitab.com/support/answers/answer.aspx?id=2588( http://it.minitab.com/support/answers/answer.aspx?id=2588)
http://it.minitab.com/support/answers/answer.aspx?id=2588)

