
方澍晨 | 撰文
旧梦 | 编辑
11月24日,石药集团开发的“SYHX1901片”用于治疗重症新冠肺炎成人患者的临床试验。
公告还提到,该药物是小分子化合物,为JAK/TYK2抑制剂,可通过抑制介导B细胞和T细胞中与炎症反应相关的信号通路上的关键靶点,抑制细胞因子风暴。
细胞因子风暴即免疫风暴是大多数新冠重症患者死亡的原因。正常状况下,免疫系统处于可控状态,不会伤害人体本身。而细胞因子风暴发生的时候,免疫系统在对抗病毒的同时,对人体也造成巨大伤害,甚至导致死亡。
石药集团已围绕新冠防治进行了多种布局。其mRNA新冠疫苗,正在进行多项临床试验。
此外,公开资料显示,石药集团在今年9月份已针对辉瑞Paxlovid的两种主要组成部分奈玛特韦(nirmatrelvir)和利托那韦(ritonavir),注册了自研产品的生物等效性(BE)试验。所谓BE实验,即用以验证仿制药和原研药效果比较的实验,前几年轰轰烈烈开展的“仿制药一致性评价”即要求仿制药企补做BE实验。
-01-
石药已对奈玛特韦、利托那韦注册临床试验
辉瑞的抗病毒口服药Paxlovid,由奈玛特韦和利托那韦两种药片组成。其中,抑制新冠病毒复制的主要是奈玛特韦。利托那韦则提供辅助,作用是保证奈玛特韦的血药浓度。
搜索“中国临床试验注册中心”网站可知,石药集团于2022年9月26日注册了奈玛特韦片的生物等效性试验,试验主办单位还包括杭州树兰医院。
按照试验注册信息,该试验的目的是:评价石药集团中诺药业生产的奈玛特韦片与Pfizer Manufacturing Deutschland GmbH生产的参比制剂奈玛特韦片的生物等效性。


图片来源:“中国临床试验注册中心”网站
公开信息显示,Pfizer Manufacturing Deutschland GmbH 即辉瑞在德国的制造公司。中诺药业是石药集团在内地投资设立的合资企业,是中国专业的抗生素原料、制剂生产基地和中国主要的非专利药物供应商,之前主打产品是阿莫西林分散片、阿莫西林胶囊。
“中国临床试验注册中心”网站还显示,2022年9月19日,石药集团还与树兰医院共同注册了利托那韦片的生物等效性试验。这一试验的受试试剂利托那韦片,生产方同样是中诺药业。


图片来源:“中国临床试验注册中心”网站

巧合的是,近日,数名石家庄方舱中的新冠病毒感染者表示,自己被发放了粉色、白色的药片,并被要求签署一则知情同意书。
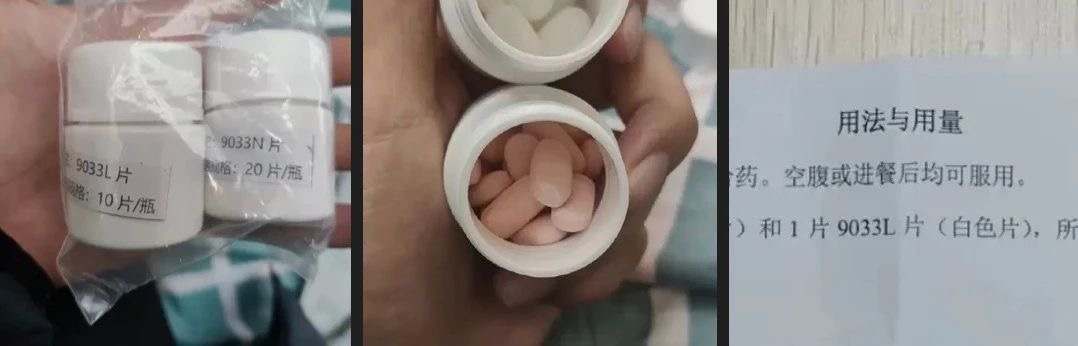
几名感染者收到的知情同意书内容显示,这是一则“评价奈玛特韦片在COVID-19成年患者中有效性和安全性”的临床试验。
目前不能确定这些网友的经历与石药集团有关联。不过,考虑到石药的大本营在河北,联合其已注册的这两项生物等效性试验,业内人士猜测,不排除一种可能:石药在牵头做其自产Paxlovid针对新冠轻症的临床试验。
不过,这两项生物等效性试验的注册联系人否认了这一猜测。她表示等效性试验还未开始、该药目前未进行其他试验,并称该药并未在石家庄做临床。树兰医院的研究负责人则表示,“与新冠相关的项目都是保密的”。
-02-
在中国,谁有权利制造Paxlovid?
2022年年初,药品专利池MPP(Medicines Patent Pool,下称MPP)授予了五家中国企业豁免专利费生产辉瑞Paxlovid的权利。
其中,九洲药业获准生产原料药,迪赛诺、华海药业、普洛药业、复星医药获准生产原料药与制剂。
值得注意的是,MPP专利池这样授权的目的,是为增加该药在中低收入国家的可及性,而中国并不在这些国家之列。以复星医药为例,该企业曾在2022年3月发布公告声明,其所获授权的内容是生产奈玛特韦的仿制药和奈玛特韦/利托那韦组合,并“在区域内(即印度、巴基斯坦、科特迪瓦等 95个中低收入国家,不包括中国)商业化许可产品及相关权利”。
换句话说,这五家药企当时只是获授权生产Paxlovid,但产品并不能在中国市场销售。
同时,由于利托那韦在中国的核心专利权已到期,这五家获得的许可并不包括利托那韦。据药监局网站,目前只有歌礼制药的利托那韦片已经过一致性评价获批上市。
歌礼已与辉瑞就这一药物的合作达成协议。2022年10月,歌礼发布公告称:“将非排他性地授权辉瑞中国在中国大陆使用歌礼的利托那韦片部分注册资料用于新冠药物PAXLOVID,并为辉瑞中国在中国大陆生产和供应利托那韦片”,有效期5年。
不过,已几乎无专利权限制的利托那韦,注定会是多家药企争夺之地。
已注册利托那韦生物等效性临床的石药中诺,就是诸多摩拳擦掌的企业之一。此外,在药物临床试验登记与信息公示平台上可以看到:石药中诺、先声、乐普等多个企业都在做利托那韦的等效性试验,不过适应症大多是HIV。
此外,更值得注意的是奈玛特韦——它还在专利保护期内。
由前述试验注册信息可知,石药已开始了对石药中诺所产奈玛特韦片的临床研究。
近日全国多地疫情加重,新冠治疗药物或许是接下来一段时间,多家药企竞争的重点。下一步,还会发生什么?除了多家药企自研产品之外,谁会成为辉瑞Paxlovid的第一个仿制者,也是值得关注的话题。
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/5Hj6wR08jNaTUTx5N6nK7A)
声明:本文内容由平台创作者发布,内容仅代表作者本人观点;如内容涉及违法、侵权等情形,请及时联系工作人员处理!工作人员微信:pckt6842。
资讯原址:https://www.ouryao.com/plugin.php?id=ts_portal&ac=view&nid=2833



