
欧洲肿瘤内科学会免疫肿瘤学(ESMO-IO)大会将在 12 月 7 日 - 9 日举行,今日其摘要已经放出。
在这次会议上,信达生物的 TIGIT 单抗 IBI939 联合 PD-1 信迪利单抗一线治疗局部晚期不可切除或转移性 PD-L1 阳性 NSCLC 的 I 期临床数据也初次公布(登记号:NCT04672369)。这也是国内继百济神州之后,第 2 款公布 PD-1 联用方案初步疗效数据的 TIGIT 单抗。
IBI939 最新临床数据 / Insight 数据库

截图来自:Insight 数据库(http://db.dxy.cn/v5/home/)
欢迎点击文末「阅读原文」,领取 Insight 数据库免费试用账号
该研究纳入了 42 例既往未经系统治疗的 PD-L1 阳性(TPS≥50%)、驱动基因阴性晚期或转移性 NSCLC 患者,按 2:1 随机分组接受 IBI939 20mg/kg 联合信迪利单抗 200mg IV Q3W 或信迪利单抗单药 200mg IV Q3W 治疗。主要终点为 ORR,次要终点包括 PFS、OS 以及安全性。
截至 2022 年 6 月 30 日,在 40 例可评估 NSCLC 患者中,TIGIT 联合疗法组相较于信迪利单抗单药组,确认的 ORR 分别为 66.7%(95% CI,46.0-83.5)vs 61.5%(95% CI,31.6-86.1)。中位 PFS 未达到(95% CI,6.8-NA)vs 6 个月(95% CI,1.4-NA),HR 为 0.43(95% CI,0.17-1.10)。
安全性方面,TRAEs 发生率分别为 85.7% vs 71.4%(各有 2 例和 5 例患者发生 ≥3 级事件),由研究者评估的免疫相关 AEs 分别为 64.3% vs 50.0%。
结果显示,IBI939 联合信迪利单抗在一线 PD-L1 阳性 NSCLC 患者中表现出改善的 PFS 获益和可控的安全性。
信达生物拥有两款 TIGIT 抗体药:单抗药物 IBI939 和 PD-1/TIGIT 双抗 IBI321。当前这两款新药均处于 I 期临床阶段。
信达生物 TIGIT 靶点新药

截图来自:Insight 数据库(http://db.dxy.cn/v5/home/)
Insight 数据库显示,IBI939 在 2019 年度就首次在国内申报临床,并于次年 4 月启动了首项临床试验。
IBI939 基本信息
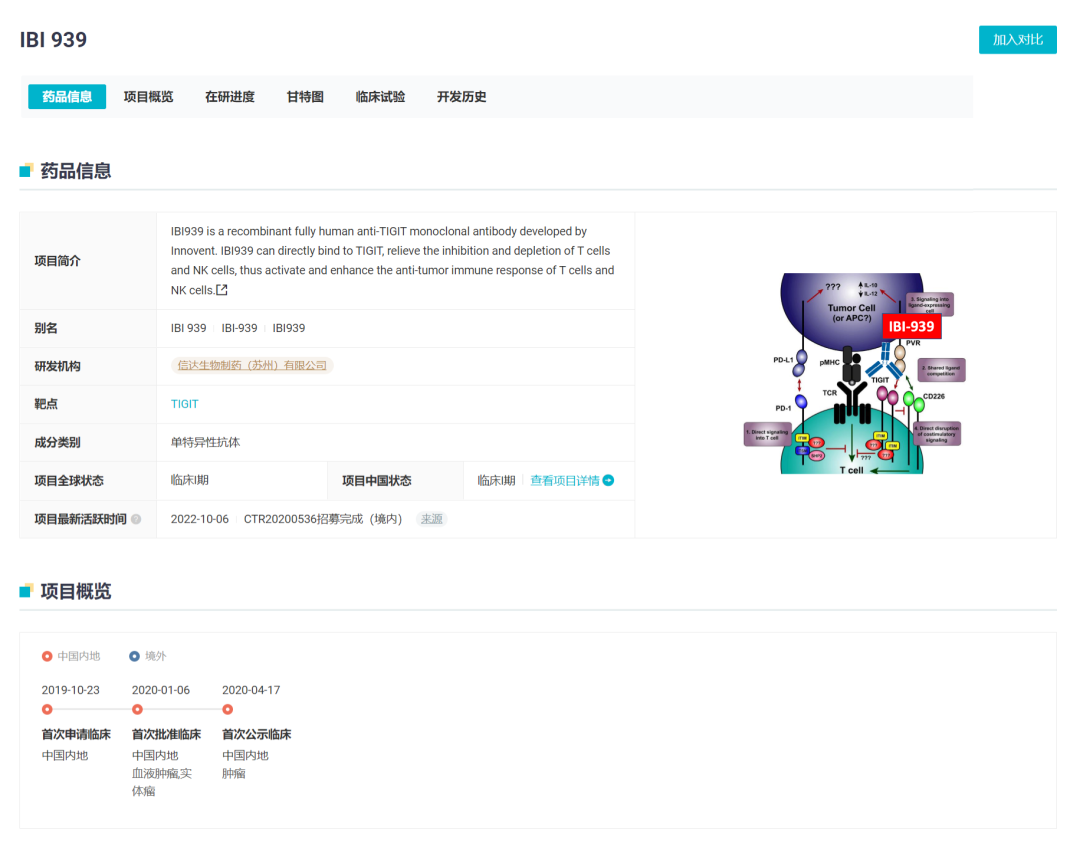
截图来自:Insight 数据库(http://db.dxy.cn/v5/home/)
免责声明:本文仅作消息分享,并不构成投资建议,也不代表 Insight 数据库的立场,文章观点仅供分享行业见解,请广大投资者谨慎。
编辑:加一
PR 稿对接:微信 insightxb
投稿:微信 insightxb;邮箱 insight@dxy.cn
点击卡片进入 Insight 小程序
国内审评进度、全球新药开发…
随时随地查!

多样化功能、可溯源数据……
Insight 数据库网页版等你体验

点击免费获取,立刻解锁!

声明:本文内容由平台创作者发布,内容仅代表作者本人观点;如内容涉及违法、侵权等情形,请及时联系工作人员处理!工作人员微信:pckt6842。



