胃癌是全球第五大常见癌症,也是癌症死亡的第三大常见原因,在东亚人群中特别常见[1,2]。
尽管大部分的胃癌都是散发性的,但仍有约10%的病例表现出家族聚集性。根据已有报道,3%~5%的胃癌病例与遗传胃癌易感性综合征有关,这其中包括遗传性弥漫性胃癌(HDGC)、胃腺癌、胃近端息肉病以及家族性肠型胃癌[3,4]。
HDGC被认为是一种具有遗传倾向的胃癌,已有研究表明25%~50%的HDGC病例都携带CDH1CTNNA1有50%~75%的HGDC病例的遗传机制还不明确CDH1的突变率也是未知的。
这就需要我国科学家来解决这个问题了。
近日,由中山大学肿瘤防治中心的徐瑞华和邱妙珍领衔的研究团队JAMA Network Open期刊发表重要研究成果[6]。
他们进行了一次回顾性队列分析,对来自284例HDGC患者的284份白细胞样本和配对的186个肿瘤样本做了全外显子以及靶向测序,发现在中国HDGC患者中CDH1的胚系变异突变率仅为2.8%,而体细胞变异突变率则有25.3%。
他们还发现,中国HDGC患者胚系变异突变率较高的一些基因与之前报道的基因并不一致,以及中国HDGC患者发病过程中可能存在遗传和环境因素的互作。

论文截图
徐瑞华团队对2002年1月1日至2018年8月31日之间,在中山大学肿瘤防治中心确诊为胃癌的10431例患者进行了回顾性分析,最终纳入分析的HDGC病例数为284(有两例HDGC患者来自于佛山第一人民医院)。
这284例HDGC患者大部分是III期或IV期患者(190例,66.9%),以及40岁前确诊弥漫性胃癌且无家族病史的患者(254例,89.4%)。患者确诊中位年龄为35岁,有161例(56.7%)为女性,中位随访期为21.7个月。仅有8(2.8%)例患者感染EB病毒,远低于之前报道的胃癌患者EB病毒感染率。患者5年存活率为61.4%,高于之前报道的散发性胃癌患者的44.1%。
接下来,研究团队对284例HDGC患者的白细胞样本以及配对的186个肿瘤样本,进行了全外显子测序。他们利用测序数据识别了患者携带的胚系变异和体细胞变异。
基于检测到的胚系变异,研究团队发现仅有8例患者携带CDH1上的变异,这与以往研究结果差异较大,并且患者携带的变异都是之前没有报道过的。这表明中国HDGC患者有着不一样的遗传背景和致病机制。
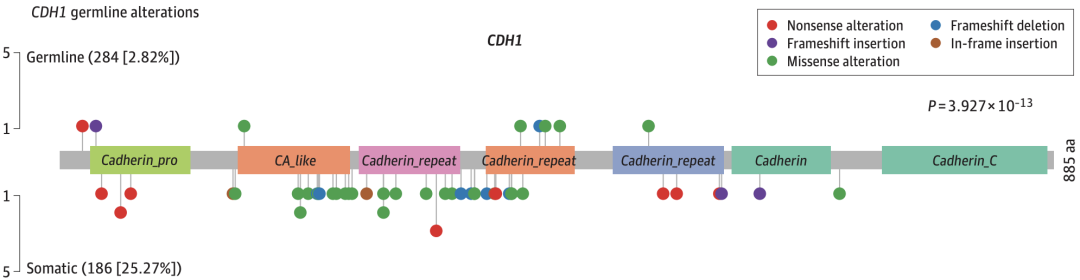
CDH1上的胚系变异和体细胞变异
除此之外,以往研究认为CTNNA1BRCA2STK11SDHBPRSS1ATMMSR1PALB2BRCA1RAD51CCDH1野生型HDGC的易感性有关。但徐瑞华团队发现,在中国HDGC患者中这些基因的突变率仍然较低,并且发生的突变与以往的报道并不一致。
在中国HDGC患者中,胚系变异突变率最高的基因是MUC4ABCA13ZNF469FCGBPIGFN1RNF213SSPO(10%),这些基因都是未曾报道过的MUC4MUC4MUC4的过表达可能通过ERBB2通路促进胃癌的恶性化。
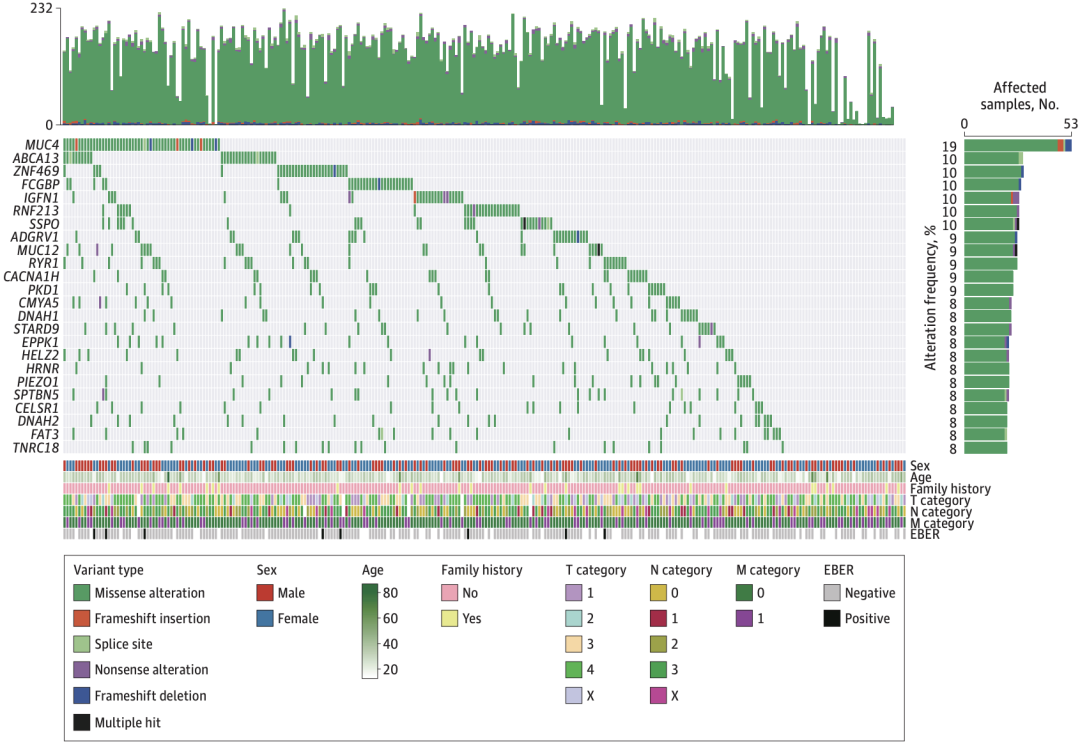
中国HDGC患者的胚系变异突变谱
利用配对的肿瘤样本,研究团队识别了186例HDGC患者的体细胞变异,突变率最高的基因是TP53(32.3%)CDH1其体细胞变异突变率却高达25.3%HRCT1KRTAP5-4等基因是显著突变基因(驱动基因)。
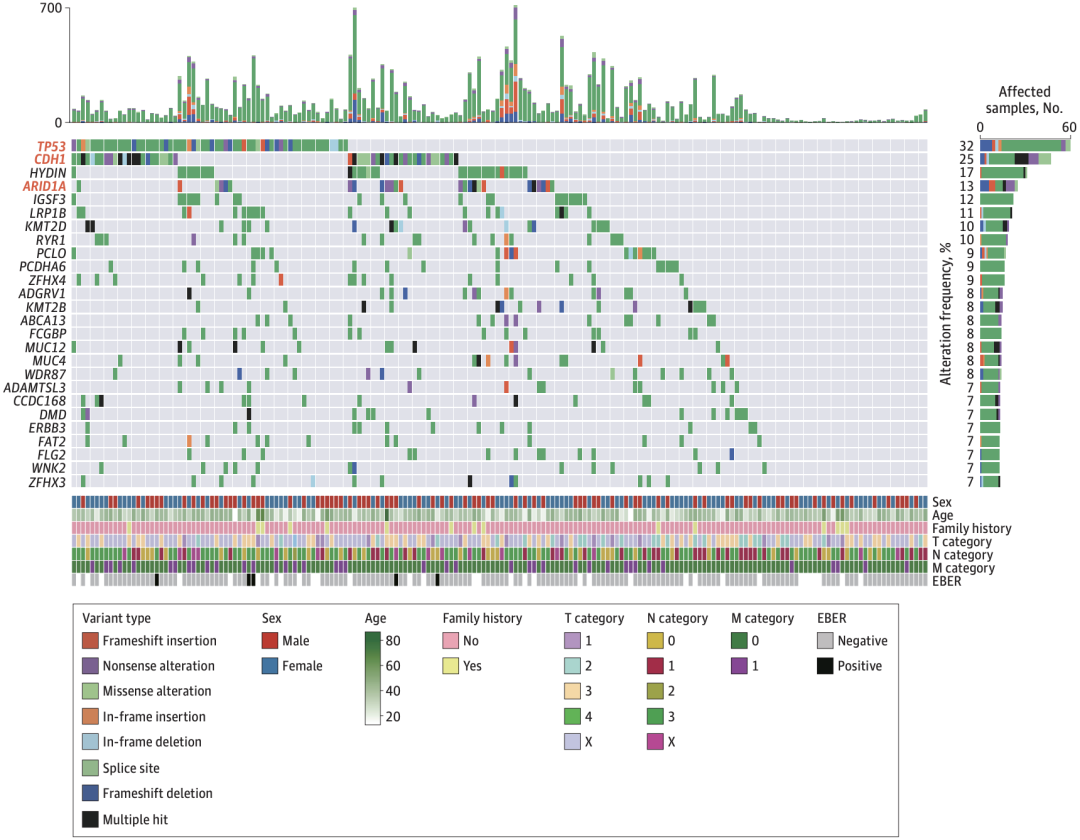
中国HDGC患者的体细胞变异图谱
随后徐瑞华团队比较了中国HDGC患者和TCGA散发性弥漫性胃腺癌(D-STAD)患者的体细胞变异负荷,发现两个队列的基因变异频率显著相关(R=0.24,P<2.2×10-16)MLLT4在D-STAD患者中的突变率是10%,而在中国HDGC患者中为0%。
研究团队还比较了两个队列在PI3K-Akt、MAPK、Wnt以及TGF-β等胃癌发生发展过程中起重要作用的通路上的体细胞变异频率,发现D-STAD患者的变异频率要高于中国HDGC患者。
在体细胞变异基础上,研究团队还分析了HDGC患者的拷贝数变异,他们发现6p22.219p13.21q21.210q21.3PTK6ERBB3PIK3CA(11.8%),这三个基因都是胃癌中已知的癌基因。
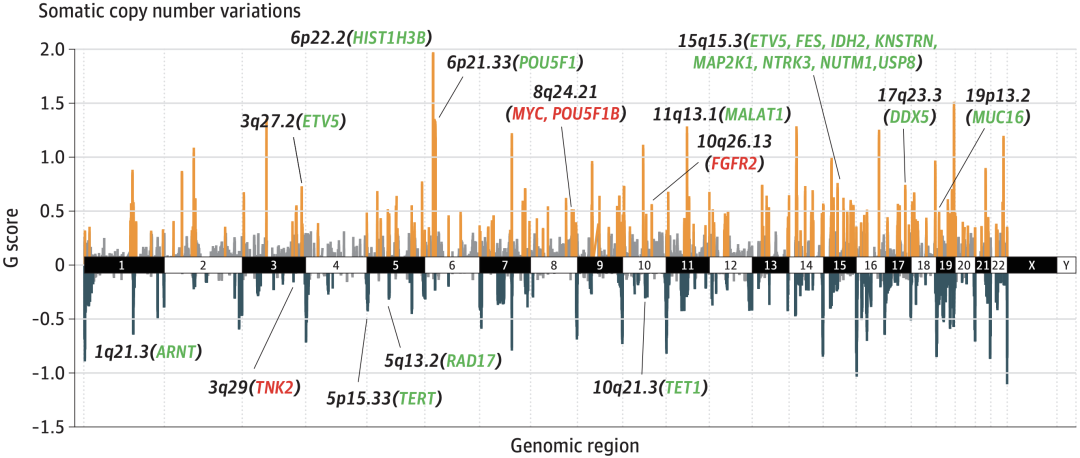
中国HDGC患者拷贝数突变频率显著较高的区域
为了探究中国HDGC患者的病因,徐瑞华团队分析了所有样本的体细胞变异特征,并与COSMIC数据库中的变异特征进行了匹配。他们发现了3个主要特征,分别是(以COSMIC特征命名):特征1(5-甲基胞嘧啶自发性脱氨)、特征5(原因未知)、特征24(黄曲霉素暴露)。表明环境因素对HDGC的发生也起到了较大作用,并且可能存在遗传和环境因素的互作关系。
最后,徐瑞华团队分析了临床预后相关的变异。在胚系变异中,他们发现有7个基因上的变异与总生存期有关,分别是SDK1HSPG2FSIP2CUBNNCKAP5FLNBMUC16。
在体细胞变异中则有大量的基因变异与总生存期有关,其中变异频率较高的基因是FGFR3ASPSCR1CICDGCR8LZTR1(HR, 2.5)。通路富集分析发现,这些基因富集于干扰素相关通路。
研究团队还通过整合OncoKB、CIViC等多个数据库,对中国HDGC患者的体细胞变异进行了临床可操作性注释。最终有125例患者的263个单核苷酸变异以及153例患者的338个拷贝数变异注释为潜在的临床可操作变异。
总的来讲,这项回顾性队列研究首次描述了中国HDGC患者的胚系变异特征,并且说明了中国患者与以往其他研究分析的患者在胚系变异特征差异较大,同时还提出了一些在中国HDGC患者中潜在的临床可操作性变异靶点,可以给未来HDGC领域研究提供参考。
参考文献:
[1] Ferlay J, Soerjomataram I, Dikshit R, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015;136(5):E359-E386. doi:10.1002/ijc.29210
[2] Chen W, Zheng R, Zeng H, Zhang S. The updated incidences and mortalities of major cancers in China, 2011. Chin J Cancer. 2015;34(11):502-507. Published 2015 Sep 14. doi:10.1186/s40880-015-0042-6
[3] Oliveira C, Pinheiro H, Figueiredo J, Seruca R, Carneiro F. Familial gastric cancer: genetic susceptibility, pathology, and implications for management. Lancet Oncol. 2015;16(2):e60-e70. doi:10.1016/S1470-2045(14)71016-2
[4] Fitzgerald RC, Hardwick R, Huntsman D, et al. Hereditary diffuse gastric cancer: updated consensus guidelines for clinical management and directions for future research. J Med Genet. 2010;47(7):436-444. doi:10.1136/jmg.2009.074237
[5] Blair VR, McLeod M, Carneiro F, et al. Hereditary diffuse gastric cancer: updated clinical practice guidelines. Lancet Oncol. 2020;21(8):e386-e397. doi:10.1016/S1470-2045(20)30219-9
[6] Liu ZX, Zhang XL, Zhao Q, et al. Whole-Exome Sequencing Among Chinese Patients With Hereditary Diffuse Gastric Cancer. JAMA Netw Open. 2022;5(12):e2245836. Published 2022 Dec 1. doi:10.1001/jamanetworkopen.2022.45836
声明:本文内容由平台创作者发布,内容仅代表作者本人观点;如内容涉及违法、侵权等情形,请及时联系工作人员处理!工作人员微信:pckt6842。



