欢迎访问『 博普智库 』制药人必备知识工具
艾司唑仑片
本品含艾司唑仑(C16H11ClN4)应为标示量的90.0%~110.0%。
【性状】本品为白色片。
【鉴别】取本品的细粉适量(约相当于艾司唑仑10mg),加乙醇10ml,振摇使艾司唑仑溶解,滤过,滤液蒸干,残渣照艾司唑仑项下的鉴别(1)、(2)项试验,显相同的反应。
【检查】有关物质 照高效液相色谱法(通则0512)( (通则0512))测定。
(通则0512))测定。
供试品溶液 取本品细粉适量(约相当于艾司唑仑2mg),加流动相溶解并稀释制成每1ml中约含0.2mg的溶液,滤过,取续滤液。
对照溶液 精密量取供试品溶液适量,用流动相定量稀释制成每1ml中约含艾司唑仑2μg的溶液。
色谱条件、系统适用性要求与测定法 见艾司唑仑有关物质项下。
限度 供试品溶液色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液主峰面积(1.0%)。
含量均匀度 取本品1片,置100 ml(1mg规格)或200ml(2mg规格) 量瓶中,加盐酸溶液(9→1000)适量,充分振摇使艾司唑仑溶解,用盐酸溶液(9→1000)稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液,照含量测定项下的方法测定含量,应符合规定(通则0941)( (通则0941))。
(通则0941))。
溶出度 照溶出度与释放度测定法(通则0931第三法)( (通则0931第三法))测定。
(通则0931第三法))测定。
溶出条件 以盐酸溶液(9→1000)100ml(1mg规格) 或200ml(2mg规格)为溶出介质,转速为每分钟100转,依法操作,经30分钟时取样。
测定法 取溶出液 10ml,滤过,取续滤液,照紫外-可见分光光度法(通则0401)( 通则0401)),在 268nm的波长处测定吸光度,按C16H11CIN4的吸收系数(如图)为352计算每片的溶出量
通则0401)),在 268nm的波长处测定吸光度,按C16H11CIN4的吸收系数(如图)为352计算每片的溶出量
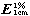
限度 标示量的80%,应符合规定。
其他 应符合片剂项下有关的各项规定(通则0101)( (通则0101))。
(通则0101))。
【含量测定】照紫外-可见分光光度法(通则0401)( (通则0401))测定。
(通则0401))测定。
供试品溶液 取本品30片,精密称定,研细,精密称取适量(约相当于艾司唑仑10mg),置100ml量瓶中,加盐酸溶液(9→1000) 60ml,充分振摇使艾司唑仑溶解,用盐酸溶液(9→1000)稀释至刻度,摇匀,滤过,精密量取续滤液5ml,置50ml量瓶中,用盐酸溶液(9→1000) 稀释至刻度,摇匀。
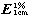
测定法 取供试品溶液,在268nm的波长处测定吸光度,按C16H11CIN4的吸收系数(如上图)为352计算。
【类别】同艾司唑仑。
【规格】(1)1mg (2)2mg
【贮藏】遮光,密封保存。
继续阅读
在线查询结果来源于2020年版中国药典,仅供参考。由专业团队进行审核校对。

